Modelo de contrato de ensaio clínico Redline Grátis




Junte-se às maiores empresas do mundo
Como enviar um PDF para assinatura eletrônica









Por que escolher pdfFiller para assinatura eletrônica e edição de PDF?

Solução multiplataforma

Armazenamento ilimitado de documentos

Facilidade de uso amplamente reconhecida

Biblioteca de modelos e formulários reutilizáveis
Os benefícios das assinaturas eletrônicas

Eficiência

Acessibilidade

Poupança de custos

Segurança

Legalidade

Sustentabilidade
Aproveite fluxos de trabalho simples de assinatura eletrônica sem comprometer a segurança dos dados

Conformidade com o GDPR

Certificado SOC 2 Tipo II

Certificação PCI DSS

Conformidade HIPAA

Conformidade com CCPA
Modelo de contrato de ensaio clínico Redline em minutos
pdfFiller permite que você crie um modelo de acordo de ensaio clínico rapidamente. A interface de arrastar e soltar descomplicada do editor garante uma assinatura rápida e fácil de usar em qualquer dispositivo.
Assinar PDFs online é uma maneira rápida e segura de validar documentos a qualquer hora e em qualquer lugar, mesmo em trânsito.
Siga as instruções passo a passo sobre como Redline o modelo de acordo de ensaio clínico eletronicamente com pdfFiller:
Adicione o documento que você precisa assinar ao pdfFiller a partir do seu dispositivo ou armazenamento em nuvem.
Assim que o arquivo abrir no editor, pressione Sign na barra de ferramentas superior.

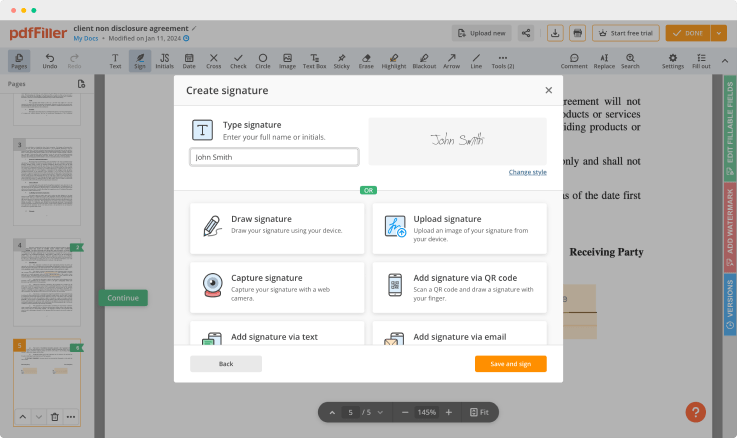
Crie sua assinatura eletrônica digitando, desenhando ou adicionando a imagem da sua assinatura manuscrita em seu laptop. Em seguida, clique em Salvar e assine.
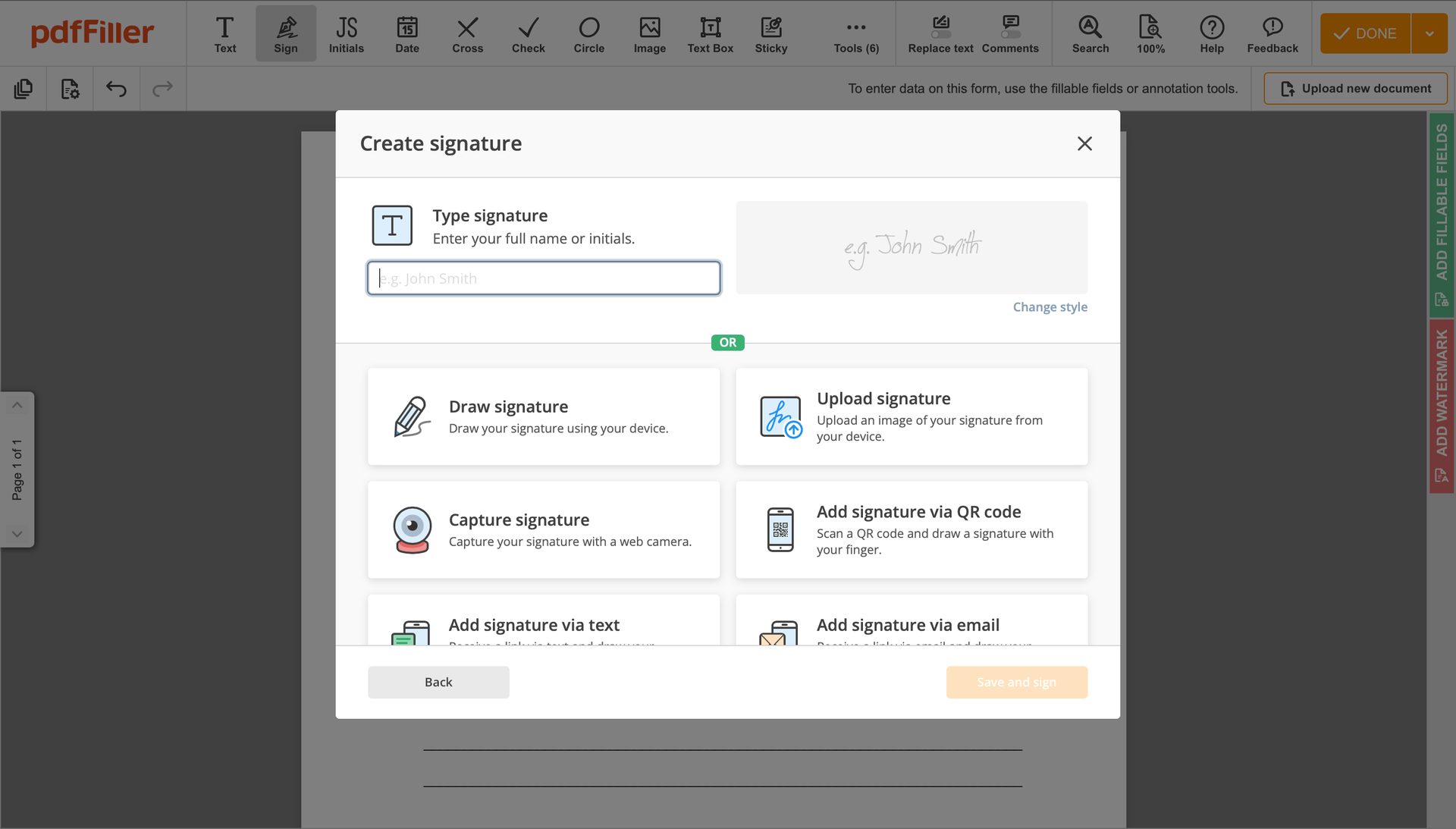
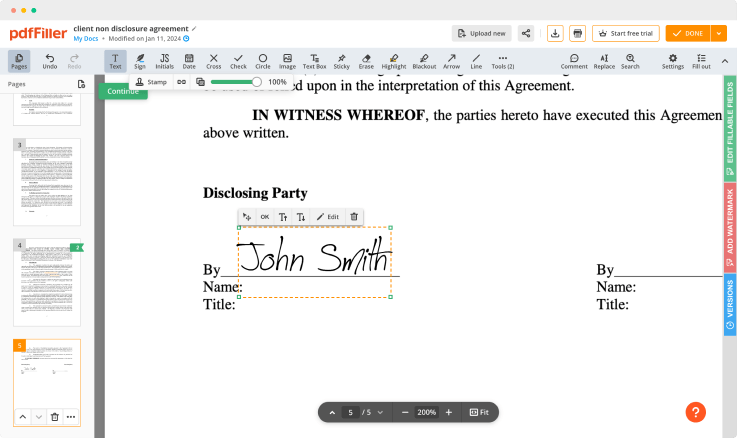
Clique em qualquer lugar em um documento para Redline Clinical Trial Agreement Template. Você pode movê-lo ou redimensioná-lo utilizando os controles no painel flutuante. Para usar sua assinatura, clique em OK.
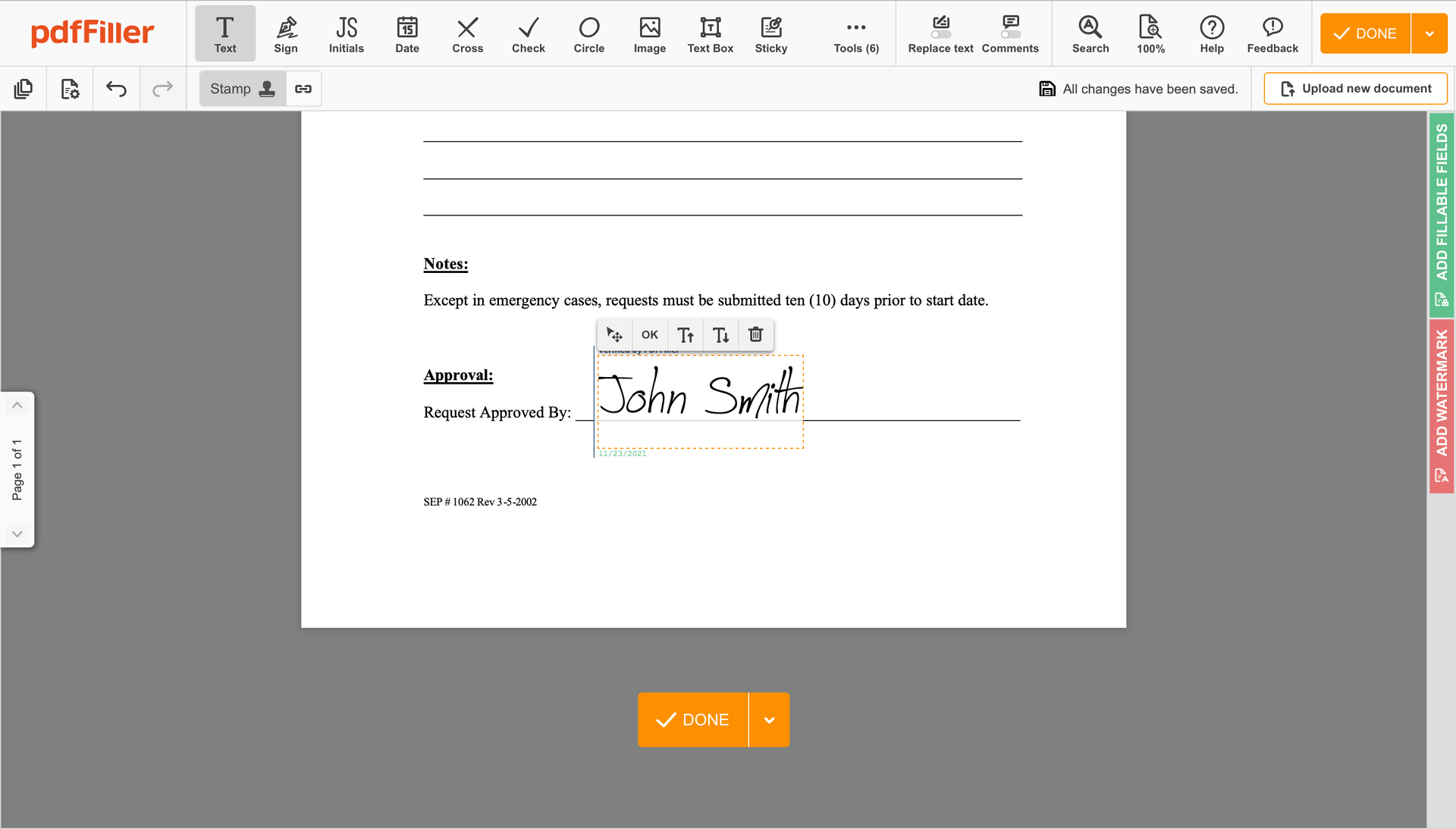
Conclua a sessão de assinatura pressionando CONCLUÍDO abaixo do formulário ou no canto superior direito.
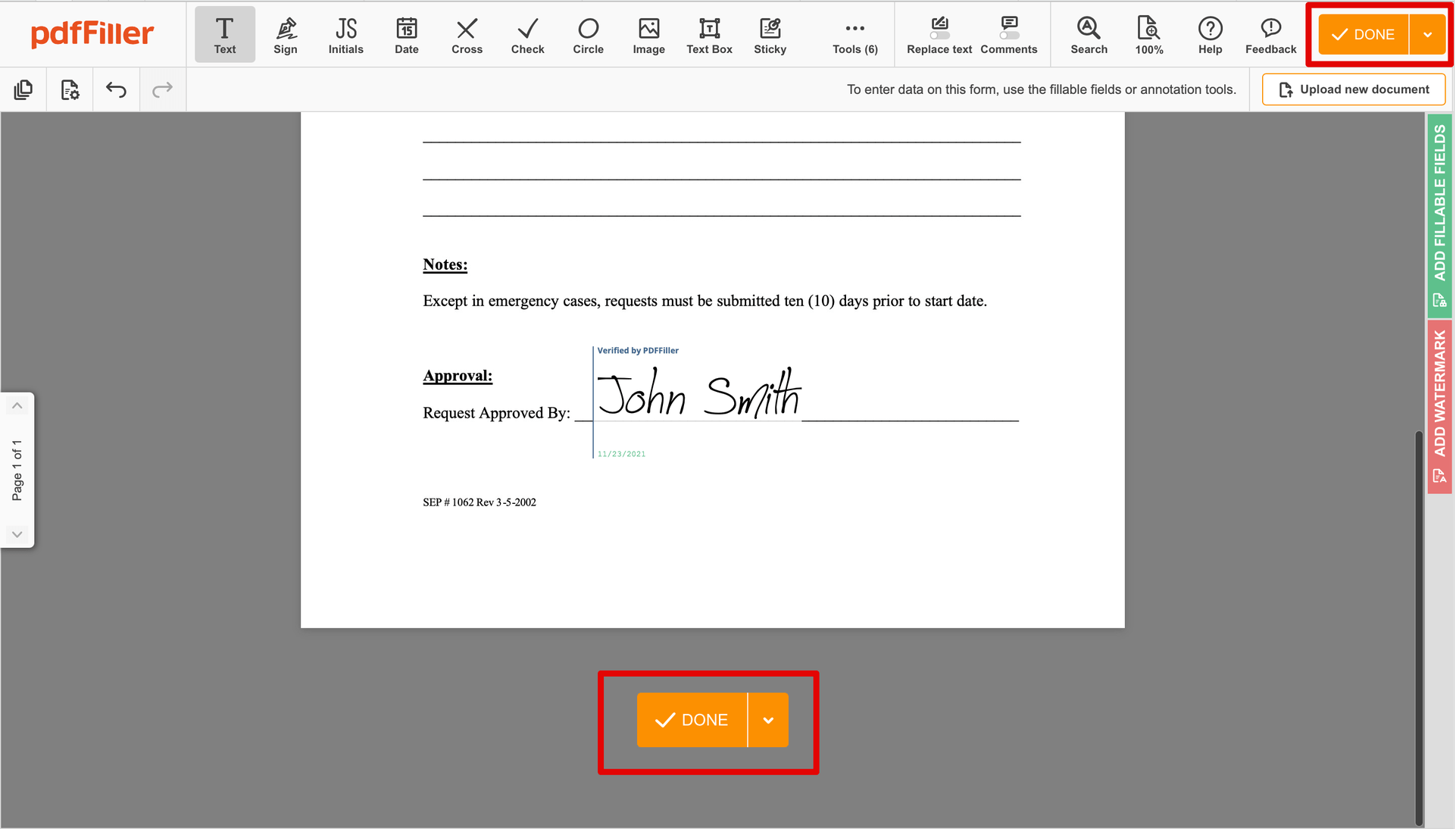
Depois disso, você retornará ao painel do pdfFiller. A partir daí, você pode baixar uma cópia completa, imprimir o documento ou enviá-lo a outras pessoas para revisão ou validação.
Preso com vários aplicativos para gerenciar documentos? Experimente esta solução completa. Utilize nossa plataforma para tornar o processo eficiente. Crie modelos de documentos completamente do zero, modifique formulários existentes e outros recursos úteis, sem sair do navegador. Você pode usar o modelo de contrato de ensaio clínico Redline com facilidade; todos os nossos recursos estão disponíveis instantaneamente para todos os usuários. Tenha uma vantagem sobre outros programas.
Como editar um documento PDF usando o editor pdfFiller:
Como usar o recurso de modelo de contrato de ensaio clínico Redline
Entendemos que usar o recurso Redline Clinical Trial Agreement Template pode ser um pouco complicado no início. Mas não se preocupe, estamos aqui para orientá-lo passo a passo no processo!
Esperamos que este guia passo a passo tenha sido útil para você. Se você tiver mais dúvidas ou precisar de ajuda, sinta-se à vontade para entrar em contato com nossa equipe de suporte. Modelo feliz!
Para Perguntas Frequentes do pdfFiller
Pronto para experimentar pdfFiller? Modelo de contrato de ensaio clínico Redline Grátis